Da sempre Mediplasma si impegna per ottenere risultati in grado di cambiare il modo radicale l'utilizzo dei dispositivi trattati!
Mediplasma s.r.l., primo spin off dell’Università del Molise, è stata fondata nel 2010 con la mission di effettuare lo studio e l’applicazione delle tecnologie plasmo chimiche al comparto biomedicale, in particolare al settore oftalmologico e a quello dei medical devices e delle endoprotesi, allo scopo di implementarne le caratteristiche chimico-fisiche, cliniche e commerciali. Soci fondatori sono il Prof. C. Costagliola (Dipartimento di Scienza per la Salute dell’Università del Molise), Plasma Solution s.r.l., e alcuni privati con specifiche competenze tecniche.
Il più importante socio di MEDIPLASMA è la Soc. PLASMA SOLUTION, spin-off dell’Università di Bari, azienda leader in Italia e in Europa per studi e ricerche in nanotecnologie plasmochimiche, la cui applicazione al settore biomedicale e dei medical devices è la mission fondante di MEDIPLASMA.
Applicazioni di tecnologie plasmo chimiche al settore oftalmologico e ai medical devices
I plasmi freddi in ambito biomedico
I processi via plasma sono utilizzati per modificare le proprietà superficiali di materiali di interesse biomedico per ottenere la migliore compatibilità con proteine, cellule e tessuti biologici in vitro o in vivo, in applicazioni nei campi dei biomateriali, dell’ingegneria tissutale, dei biosensori, e dei bio reattori.
Ad esempio, mediante processi PE-CVD o di trattamento via plasma è possibile modificare la superficie di polimeri a carattere idrofobo innestando specifici gruppi chimici polari che aumentano l'adesione cellulare al materiale, migliorando l’integrazione di protesi con i tessuti circostanti. Al contrario, i coating PEO(PoliEtilenOssido)-like, con caratteristiche hydrogel simili ai polimeri PEG e PEO, possono essere depositati via plasma in condizioni di bassa frammentazione da monomeri caratterizzati da unità -OCH2CH2- (EtilenOssido) per ottenere proprietà anti-adesive, non fouling, verso proteine, cellule e batteri. Questi coating sono di grande utilità quando depositati su dispositivi biomedici e sensori che devono rimanere “puliti” in ambiente biologico, sui quali è necessario evitare l’adesione di biomolecole.
Superfici adesive e non fouling possono essere alternate via plasma in pattern micrometrici per produrre dispositivi e lab-on-chip.
Ottimizzando i processi in reattori opportunamente configurati è possibile depositare via plasma coating idrofili nano-compositi contenenti argento, resistenti alla contaminazione batterica, su dispositivi biomedici, cateteri, protesi e altre superfici. Questi coating rilasciano, in ambiente acquoso, ioni Ag+ antibatterici in quantità controllabile nel tempo con le caratteristiche strutturali del coating, a loro volta ottimizzate nel processo di deposizione.
MEDIPLASMA detiene il 75% della titolarità di una invenzione riguardante tale specifica applicazione plasmo chimica, per la quale è in fase di rilascio un brevetto internazionale, come illustrato dettagliatamente in seguito
I processi via plasma possono inoltre modificare la composizione superficiale di membrane (con coating a carattere idrofilo o idrofobo o non fouling, o mediante l'innesto di gruppi chimici per l'immobilizzazione di biomolecole o di catalizzatori, senza alterarne le caratteristiche di trasporto, porosità e permeabilità.
Superfici idrofile possono essere sintetizzate via plasma su polimeri idrofobi sia tramite grafting di gruppi polari, o per deposizione di coating idrofili. In entrambi i casi le superfici modificate presentano gruppi polari (es. -NH2, -COOH, -OH) e, di conseguenza, maggiore bagnabilità e migliore compatibilità con cellule, tessuti e fluidi biologici. La presenza di questi gruppi funzionali permette, già da sola, di aumentare l'adesione cellulare alla superficie dei materiali; inoltre, questi gruppi possono essere utilizzati per immobilizzare molecole biologiche e ottenere risposte specifiche da tipi cellulari ben definiti. L’immobilizzazione di peptidi e saccaridi, in particolare, permette di “mimare” un ambiente biologico più adatto (Extra Cellular Matrix, ECM) all’adesione e al comportamento biologico di cellule primarie specifiche, ed è una strategia usata in bioreattori e organi artificiali.
Via plasma è possibile depositare coating caratterizzati da micro/nano strutture superficiali. Essendo le cellule sensibili anche alla morfologia superficiale dei materiali, oltre che alla composizione chimica, questa caratteristica offre una possibilità in più alle tecnologie plasmo chimiche per ottimizzare l’adesione cellulare su superfici di interesse biomedico.
Reattori plasmo chimici
Una volta studiato in laboratorio, il processo plasmochimico va trasferito all’applicazione industriale, sulla superficie di campioni reali, con la riproducibilità e le portate tipiche dei processi produttivi. Una consociata di MEDIPLASMA produce reattori plasmochimici con il processo ottimizzato ad hoc sul substrato del cliente. In genere, per capire l’effetto dei parametri sperimentali (potenza, pressione, etc.) sul processo, gli studi vengono compiuti prima su substrati piani, poi sui campioni reali. Per il trasferimento dei processi sui campioni reali, anche di grandi dimensioni (es. lastre di vetro per edilizia) è possibile costruire reattori batch e in continuo per trattare in modo omogeneo ogni tipologia di substrato: polveri nanometriche, granuli, nastri (reattori roll-to-roll), fili, tubi, cateteri, etc.
Descrizione di invenzione industriale avente per titolo
Realizzazione di coating nanometrici antibatterici a rilascio controllato di agente battericida
(Patent pending. N. WO 2013/021409 A8)
RIASSUNTO
La presente invenzione si riferisce alla realizzazione di rivestimenti idrofili con proprietà antibatteriche da rilascio controllato, uniforme e duraturo di ioni Ag+ in ambienti umidi. È stato dimostrato “in vitro” che coating depositati via plasma con struttura simile ai polimeri polietilen-ossido (PEO-like) scoraggiano l’adsorbimento di proteine e l’adesione cellulare; coating simili, quando contengono cluster di argento, hanno anche un netto effetto battericida, per esempio nei confronti di batteri P.aeuriginosa e S.epidermis.
Essa si basa sullo studio di processi PE-CVD (Plasma Enhanced Chemical Vapor Deposition) per la deposizione di film sottili (20 nanometri - 1 micron) organici, inorganici o nano compositi. Variando il gas di alimentazione del plasma e le condizioni di deposizione si possono ottenere film sottili a composizione variabile in continuo con le condizioni di deposizione, dalle caratteristiche assolutamente uniche, tra i quali coating organici con caratteristiche “non fouling” di resistenza, cioè, all’adesione e alla contaminazione con sostanze organiche e biologiche in ambiente acquoso (con “monomeri” tipo glicoli etilenici). Accoppiando un processo di sputtering ad un processo PE-CVD convenzionale, è possibile produrre coating nanocompositi, costituiti, cioè, da cluster nanometrici (metallici, ceramici o polimerici) inclusi in film sottile.
STATO DELLA TECNICA
Sono note le tecniche di deposizione via plasma di film con proprietà repellenti per materiale biologico. Sulla superficie di un materiale che abbia affinità per componenti biologici (proteine, cellule, batteri, funghi, alghe), una volta che questo sia posto in ambiente non sterile, si ha la formazione di un biofilm (fouling) di composizione variabile che può promuovere l’adesione e la crescita di batteri e spore. La presenza delle biomolecole può alterare le prestazioni del dispositivo (sensore, filtro, reattore, protesi) con cui il materiale è fabbricato. Per i dispositivi biomedici come protesi vascolari e cateteri, il fouling può degenerare nella colonizzazione batterica, quindi in infezioni, degradazione dei materiali e rimozione delle protesi infette, con conseguenze anche gravi sui pazienti.
E’ stata anche studiata la possibilità di conferire al film caratteristiche antibatteriche, mediante l’utilizzazione di fini dispersioni, in globuli di circa 2-4 nm, di argento, un antibatterico noto fin dall’antichità, inclusi nella matrice di un film non fouling, durante un unico processo di deposizione. L’efficacia antibatterica (diminuizione di popolazione batterica di 6 ordini di grandezza) è stata provata su linee di batteri Staphilococcus Aureus e di Pseudomonas Aeruginosa.
Il rilascio degli ioni argento avviene, però, in maniera non controllata e rapidamente decrescente, in funzione della concentrazione dei globuli nel coating, della natura e spessore dello stesso e delle proprietà chimico-fisiche del mezzo in cui il dispositivo è collocato.
L’attività di ricerca di MEDIPLASMA unitamente alla consociata PLASMA SOLUTION (spin-ff dell’Università di Bari) e di UNIBA in questo settore ha permesso di mettere a punto un dispositivo a rilascio controllato, uniforme e duraturo, non citotossico, che costituisce l’essenza del presente brevetto, la cui titolarità compete per il 75% a MEDIPLASMA e per il 25% alla Università di Bari.
FONDAZIONE SCIENTIFICA “POTITO” – UNIVERSITA’ DEL MOLISE
Di seguito si riportano le sintesi di tre studi effettuati dalla Fondazione scientifica POTITO sulle proprietà chimico-fisiche, microbiochimiche ed immunologiche del coating antibatterico in corso di brevettazione internazionale. Gli studi completi sono disponibili a richiesta degli interessati.
Studio di caratterizzazione chimico-fisica e sulle modalità del rilascio di ioni argento da coating plasmo chimici nano strutturati, depositati su campioni non commerciali di lentine intraoculari (Prof. Luigi Ambrosone).
Lo studio è stato effettuato su campioni non commerciali di lentine intraoculari, allestite presso la Società Plasma Solution (spin off dell’Università di Bari) e ricoperte con rivestimenti di spessore nanometrico a rilascio controllato di ioni argento, per il quale è stato depositata domanda di brevetto nazionale ed internazionale.
Sono stati creati diversi sistemi modello da utilizzare come migliorativi, o sostitutivi, dei dispositivi per la visione (lentine intraoculari, lenti a contatto). Nella fattispecie, sono stati ricoperti dei quadrati di polietilentreftalato (PET), della grandezza di circa 1 cm per lato, con uno strato nanomolecolare di Ag, con spessore del ricoprimento nel range 10 – 100 nm.
Scegliendo opportunamente i parametri del processo “plasmo-chimico” può essere controllata sia la quantità di argento inglobata sia il grado di reticolazione della fase organica in cui quella inorganica (argento) è finemente dispersa.
Una prima tipologia di esperimenti ha dimostrato che il PET senza film di Ag immerso in 100 ml di una soluzione fisiologica, a temperatura di 37°C dopo due mesi circa non rilasciava in soluzione Ag ( in qualsiasi forma); la sensibilità dell’apparecchio era 10 ppb (parti per bilione).
L’effetto antibatterico dell’argento, quindi, può essere modulato variando le caratteristiche del film depositato; pertanto, sono state preparate tre diverse tipologie di campioni. Le loro caratteristiche sono riportate nella Tab. 1. Si tratta di tre tipologie di campioni che consistono, essenzialmente, in film di Ag non ricoperto da nessun altro film e film di Ag ricoperto da un ulteriore strato di polietilenossido (PEO) a diverse percentuali.
Tab.1 Diversi tipi di campioni preparati con la tecnica APS su quadrati di lato 1 cm di PET
TIPO I
Film Ag/PEO-like (Ag 5%) assenza di film protettivo
TIPO II
Film Ag/PEO-like (Ag(5%)bfilm protettivo (PEO 70%)
TIPO III
Film Ag/PEO-like (Ag 5%) film protettivo (PEO 30%)
Sono state effettuate due tipi di analisi: morfologico/strutturale e chimico-fisiche. Le prime sono state condotte direttamente sui campioni solidi mediante Microscopia Elettronica a Scansione (SEM) e spettroscopia a raggi X (XRD); le seconde sono state effettuate sulla soluzione liquida in cui i campioni erano immersi per valutarne le proprietà di rilascio.
Parte Prima - Misure morfologiche
- Analisi SEM
Le analisi sono state eseguite con un potente strumento prodotto dalla Zeiss.
- Diffrazione di raggi X (XRD)
Sul microscopio è presente un rivelatore (Oxford Instruments) per analisi EDS, Energy Dispersive X-ray. L’identificazione dei picchi ottenuti è stata svolta grazie a confronti con spettri presenti nell’ampia banca dati del software.
Preparazione dei campioni
I campioni erano preparati ricoprendo, mediante la tecnica dei plasmi, dei provini di PoliEtileneTereftalato (PET) di forma quadrata con lato di 1cm. Le proprietà finali del materiale preparato dipendono sia dalla quantità di Argento e altri composti utilizzati per il ricoprimento dei provini, sia dalle modalità con cui essi sono ricoperti. Pertanto tre tipologie di provini con diverse caratteristiche superficiali erano studiati.
1) Tipo I, contrassegnato dal colore rosso, costruito ricoprendo il provino con un film di Argento/Polietilenossido (PEO) al 5% di Ag. Il film è lasciato libero ovvero senza nessuna ulteriore copertura.
2) Tipo II, contrassegnato dal colore blu, costruito ricoprendo il provino con un film di Argento/Polietilenossido (PEO) al 5% di Ag. Il film è ulteriormente ricoperto con un ulteriore film di PEO al 70%.
3) Tipo III, contrassegnato dal colore nero, costruito ricoprendo il provino con un film di Argento/Polietilenossido (PEO) al 5% di Ag. Il film è ulteriormente ricoperto con un ulteriore film di PEO al 30%.
Se si confrontano i risultati degli spettri per le tre tipologie di campioni si nota subito come i campioni con la ulteriore ricopertura di PEO esibiscono una minore percentuale di Ag in superficie. Questo risultato può essere spiegato tenendo presente che la capacità di penetrazione degli elettroni nel SEM è sempre la stessa nei tre campioni, ma dato che il provino di tipo I non ha lo strato di PEO di ricopertura, la concentrazione degli atomi Ag in questo risulta più elevata. In altre parole, la quantità di argento contenuta nel primo strato viene riferita ad un volume all’incirca doppio, corrispondente all’insieme dei due strati sovrapposti.
Parte seconda - Misure di rilascio
Metodo sperimentale per la determinazione dell’argento in soluzione acquosa
L’argento rilasciato dai campioni a diversi tempi era determinato mediante spettrofotometria di assorbimento atomico. Secondo tale metodo l’argento viene determinato per iniezione diretta di un campione nel fornetto di grafite di uno spettrofotometro ad assorbimento atomico.
Cinetica di rilascio di Ag in soluzione a pH 7.2 Temperatura 37.0°C.
I tre tipi campioni si comportano in modo diverso, a parità di tempo di osservazione. In termini assoluti il tipo III rilascia meno Ag di quanto non facciano il Tipo I e II. Il tipo I sembra raggiungere un plateau intorno a 10 giorni, poi ri-cresce con velocità diversa. In ogni caso rilascia la più alta concentrazione di Ag. Per i campioni di tipo II la curva di rilascio ha un andamento simile al tipo I, sebbene la concentrazione di Ag sia leggermente più bassa. I campioni di tipo III esibiscono una curva di rilascio completamente diversa, cresce con continuità fino a raggiungere un plateau.
I campioni di tipo I sono caratterizzati dall’assenza del film protettivo cosicché, lo strato di Ag è a diretto contatto con la soluzione. In tal caso, le molecole di acqua possono liberamente entrare nel film, gonfiandolo (swelling) e favorendo la diffusione dell’Ag verso la soluzione bulk. E’ bene precisare che l’argento può o diffondere come Ag o trasformarsi in ione (Ag+) generando una sospensione di argento colloidale. Una siffatta interpretazione spiega anche la risalita della curva rossa. Infatti, le molecole di acqua devono diffondere all’interno del film prima che gli atomi di Ag possano rilasciare; quando la concentrazione di acqua all’interno dello strato è sufficientemente elevata, aumenta la concentrazione di Ag che viene “ staccata” dal film.
I campioni II e III sono formati da uno stesso strato di Ag (5%) e protetti con film di PEO a diverse concentrazioni percentuali. La differenza di comportamento mostrato nel grafico, quindi, deve essere attribuita alla diversa concentrazione di PEO utilizzata per formare lo strato protettivo. Una ulteriore osservazione evidente dal grafico è che il campione III, non solo presenta la minore concentrazione di Ag, ma anche la più bassa velocità di rilascio del metallo. Queste due evidenze sperimentali possono essere interpretate sulla base della struttura e conformazione delle macromolecole di PEO.
E’ ben noto che il PEO in opportune condizioni chimico fisiche raggiunge una configurazione tale che l’angolo diedro CH2-O-CH2 assuma un valore simile a quello della molecola d’acqua H-O-H. Sotto tali condizioni la idrofobicità del PEO è minimizzata e le molecole di acqua possono essere accomodate all’intero dei cluster macromolecolari. I dati riportati nel grafico, quindi, indicano che ad una concentrazione superficiale del 70% il PEO raggiunge una configurazione tale da ospitare molta più acqua e quindi consente la “controdiffusione” di più molecole di Ag. Al contrario, nella concentrazione al 30% i cluster sono molto più compatti e l’acqua diffonde molto più difficilmente; si raggiunge quasi subito (relativamente agli altri campioni) lo stato di equilibrio.
FONDAZIONE SCIENTIFICA “POTITO” – UNIVERSITA’ DEL MOLISE
Studio per la valutazione dell’attività antimicrobica sulle superfici di contatto, a seguito del rilascio di ioni argento da coating plasmo chimici nano strutturati, depositati su campioni non commerciali di lentine intraoculari. (Prof. Roberto DI MARCO)
Generalmente, l’intervento di cataratta non comporta particolari rischi e ad eccezione di alcuni pazienti che non hanno recuperato più la vista la percentuale di successi è superiore al 95%. Una complicanza è rappresentata dalla cosiddetta cataratta secondaria che si verifica quando avviene l’opacizzazione della capsula posteriore del cristallino operato. Più gravi, invece, sono le complicanze infettive che comportano un immediato reintervento prima che i germi possano contaminare la retina e creare un danno irreparabile.
L’endoftalmite è la complicanza più temuta di ogni chirurgia oculare, perché se non trattata tempestivamente può portare alla completa perdita della vista.
PRESIDI DI VISIONE
Vista la pericolosità delle infezioni post-chirurgiche è necessario prevenire quest’ultime e un buon metodo sarebbe quello di effettuare l’intervento chirurgico della cataratta con l’inserimento di una lente artificiale dotata di ioni di argento in grado di combattere l’eventuale insorgenza di infezioni.
L’attività antibatterica dell’argento è ben nota in letteratura e numerose sono le sue applicazioni nella pratica clinica. Gli ioni argento posseggono proprietà biologicamente attive, normalmente utilizzati in formulazioni contenenti argento sottoforma di sali, ossido, chelati, e ioni. Queste formulazioni danno origine a complessi metallo-organici e composti insolubili con i gruppi sulfidrilici (ad es., residui di cisteina) delle pareti cellulari di batteri e funghi inattivando enzimi responsabili del metabolismo energetico e del trasporto degli elettroni. Gli ioni argento bloccano anche il trasporto degli elettroni tra citocromo reduttasi e citocromo-ossidasi e tra NADH e succinato deidrogenasi.
L’attività antimicrobica degli ioni argento è stata osservata a concentrazioni che vanno da 0.1 nM a ~ 5 μM, mentre la tossicità cellulare in vitro è stata osservata a concentrazioni che si avvicinano ai 12 μM.
L’effetto antibatterico dell’argento, quindi, può essere modulato variando le caratteristiche del film depositato, pertanto, sono state preparate tre diverse tipologie di campioni. Si tratta di tre tipologie di campioni che consistono, essenzialmente, in film di Ag non ricoperto da nessun altro film e film di Ag ricoperto da un ulteriore strato di polietilenossido (PEO) a diverse percentuali.
Sebbene l’argento sia ampiamente sfruttato come battericida, ad alte dosi può produrre discreta tossicità, pertanto i dispositivi, per essere utilizzati nell’organismo umano, devono essere stabili ovvero non rilasciare eccessive quantità di Ag. Le concentrazioni di Ag devono essere al di sotto del limite di tossicità (50-100 μg/L).
RISULTATI – Inibizione da contatto
Per tutti i ceppi saggiati è stato registrato un abbattimento totale della carica dopo 3 ore di contatto con il supporto ottico trattato con l’argento. Solo per il ceppo di S. aureus inoculato ad una concentrazione di 1x104 ufc/mL si osservava a 3 ore un dimezzamento della carica pari a circa 5x103 ufc/mL e solo a 6 ore si è registrato un azzeramento della stessa.
RISULTATI – Prove di diffusione in mezzo semi solido
In linea generale il preparato sembra perdere le proprietà antimicrobiche già nelle porzioni di agar contigue e negli stati al di sotto della lente dimostrando quindi una scarsissima diffusibilità in un mezzo semi solido. In uno degli esperimenti una lieve riduzione della carica batterica di B. clausii è stata osservata nel contesto dell’agar posto al di sotto della lente.
CONCLUSIONI
Studi in vitro su batteri resistenti agli antibiotici trattati con nitrato d’argento, sulfadiazina d’argento e medicazioni attive hanno dimostrato come l’efficacia antibatterica di queste ultime fosse più elevata, con un’attività più a largo spettro ed un tasso di efficacia maggiore rispetto alle prime due alternative.
Le evidenze disponibili suggeriscono che la maggioranza dei prodotti a rilascio continuativo di ioni argento sono efficaci contro ceppi resistenti alla meticillina ed alla vancomicina e sino ad ora non è stata ancora mostrata alcuna resistenza all’argento.
La carica batterica delle lesioni negli esseri umani è un problema persistente nella gestione delle stesse, soprattutto nelle infezioni post-operatorie. I prodotti a rilascio continuato di argento hanno un’azione battericida eo batteriostatica.
I materiali incorporati alle moderne medicazioni a base di argento quali idrocolloidi, schiume ed altri polimeri sono un aiuto nella gestione delle infezioni e modulano, inoltre, il rilascio di ioni argento.
La modalità del meccanismo d’azione dell’argento non è ancora stata chiarita del tutto. Oggi si parte dal presupposto che siano gli ioni argento e non gli atomi a sviluppare l’effetto germicida, dato che l’argento metallico non è molto reattivo. E in ambiente liquido l’argento metallico, quindi anche le particelle colloidali, rilasciano costantemente ioni argento in grado di esplicare la loro azione antimicrobica.
Gli ioni argento reagiscono molto intensamente con alcuni gruppi chimici contenenti zolfo (gruppi sulfidrici o titolici). In tal modo si verificano due fenomeni: la distruzione di strutture cellulari e l’inattivazione di enzimi. Ma questi ultimi prendono parte a innumerevoli meccanismi all’interno delle cellule, senza i quali la vita non sarebbe possibile. Se la loro funzione viene ostacolata o l’enzima stesso viene distrutto, vengono ostacolati anche dei processi vitali di quei germi patogeni, che di conseguenza muoiono.
L’argento esercita la propria azione anche sugli acidi nucleici dei batteri, importanti componenti delle loro informazioni genetiche (DNA e RNA). Evidentemente il legame dell’argento impedisce la proliferazione del plasma germinale poiché l’RNA o il DNA viene stabilizzato. In questo modo si impedisce la duplicazione delle informazioni genetiche necessarie per la moltiplicazione cellulare. Una tale interazione deve essere quindi corresponsabile, se non addirittura determinante per l’effetto antibatterico.
Nel nostro studio dimostriamo che il preparato di tipo III mostra una efficacia batterica sui ceppi da noi saggiati. La velocità di Killing relativa ai preparati rispetto ad altre metodologie è estremamente efficace mostrando un effetto entro le tre ore. I risultati da noi ottenuti mostrano una efficienza ad ampio spettro sia sui bacilli Gram negativi che sui cocchi Gram positivi, nonché germi anaerobi.
E’ opportuno enfatizzare il fatto che gli ioni argento non diffondono nel mezzo semi solido, che nel nostro sistema è rappresentato dall’agar e che per diffusibilità e sistema acquoso potrebbe essere simile al vitreo. L’azione antibatterica sarebbe pertanto limitata alle strutture limitrofe. Tale proprietà presenta vantaggi legati all’assenza di effetti dannosi a carico delle strutture retiniche, con attenuazione delle trasmissioni nervose.
FONDAZIONE SCIENTIFICA “POTITO” – UNIVERSITA’ DEL MOLISE
Valutazione degli effetti, su cellule del sistema immunitario, dell'esposizione a superfici trattate con Ag/PEO-Like. (Prof. Antonio PORCELLINI)
Metodologia e materiali utilizzati.
Il set di esperimenti presentati misura la proliferazione e l'attivazione funzionale indotta in leucociti umani normali dall'esposizione ad un prisma di Polietilene Tereftalato (PET). I prismi di PET usati sono stati trattati con diverse formulazioni di Ag/PEO-Like.
Lo scopo del test è molteplice:
1) misurare l'abilità del trattamento superficiale Ag/PEO-Like ad indurre proliferazione leucocitaria mediante l'attivazione dei recettori per l'immunità innata.
2) misurare l'interferenza dell'esposizione ai prismi di PET con trattamento superficiale Ag/PEO-Like sulla fisiologica proliferazione leucocitaria innescata dall'esposizione ad un classico ligando per il TLR3, l'LPS.
3) misurare l'interferenza sulla proliferazione leucocitaria innescata dall'esposizione ad un anticorpo monoclonale in grado di attivare i linfociti tramite interazione con i componenti CD3 del complesso recettoriale TCR.
4) misurare l'abilità del trattamento superficiale Ag/PEO-Like ad indurre attivazione leucocitaria.
5) misurare l'interferenza sull'attivazione leucocitaria indotta all'esposizione ad un anticorpo monoclonale in grado di attivare i linfociti tramite interazione con i componenti CD3 del complesso recettoriale TCR.
Tutti i test sono stati effettuati utilizzando un prisma di Polietilene Tereftalato (PET) inserito all'interno delle piastre di coltura in Polistirene in cui sono state coltivate le cellule per tutto il periodo dell'esperimento. Sono stati utilizzati prismi a base quadrata dello spessore di 1 mm con superficie di 1 cm2 (1 cm di lato). Le capsule per colture cellulari erano del modello "multiwell" a 24 pozzetti circolari del diametro di 15 mm ciascuno in grado di accogliere un singolo prisma per pozzetto che ne occupa il 50% della superficie.
I prismi in PET sono stati sottoposti a tre diversi trattamenti superficiali con Ag/PEO-Like. I trattamenti sono stati effettuati su una sola delle due facce di base dei prismi. Le facce trattate sono state rivolte verso l'alto quando i prismi sono stati collocati nei pozzetti così da offrire la massima superficie trattata al diretto contatto con le cellule.
I differenti trattamenti, di seguito indicati con le lettere A, B e C, differiscono per i seguenti parametri:
Tipologia "A" - doppio film di spessore nanometrico: primo film di Ag/PEO-Like (Ag: 5%) a sua volta ricoperto con un film barriera di PEO-Like (carattere PEO 70%).
Tipologia "B" - doppio film di spessore nanometrico: primo film di Ag/PEO-Like (Ag: 5%) a sua volta ricoperto con un film barriera di PEO-Like (carattere PEO 30%).
Tipologia "C" - singolo film, di spessore nanometrico, di Ag/PEO-Like (Ag: 5%)
Per ogni tipologia di trattamento di superficie sono stati realizzati 30 prismi che sono stati utilizzati per effettuare 3 test indipendenti in triplicato. Come controllo sono stati utilizzati altrettanti prismi di PET non sottoposti ad alcun trattamento superficiale.
Risultati del test:
Test di proliferazione leucocitaria. La proliferazione dei PBMCs è stata valutata mediante incorporazione di timidina triziata. L'esposizione alla timidina per 6 ore è avvenuta 48 ore dopo la messa in coltura e 6 ore prima dell'effettuazione del dosaggio.
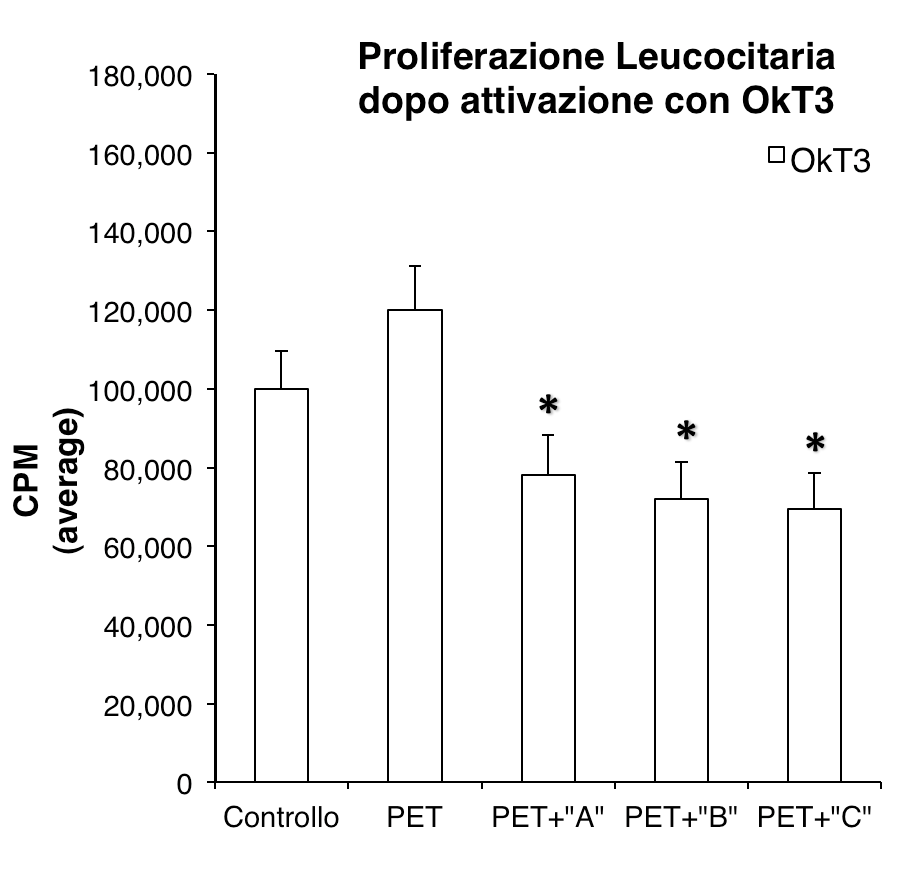
La figura 1 mostra i livelli di incorporazione di timidina tritiata in cellule PBMC non stimolate e coltivate per 60 ore in presenza di un prisma di Polietilene Tereftalato (PET) adagiato sul fondo del pozzetto. Il controllo è rappresentato da cellule coltivate in pozzetti liberi da PET. I prismi di PET sono stati trattati in superficie con i protocolli indicati nei metodi ed identificati come "A", "B" o "C" .
Essendo i livelli di incorporazione molto bassi e le cellule poco o nulla proliferanti il risultato di questo test consente di affermare che nessuno dei trattamenti superficiali conferisce ai prismi di PET qualità attivanti la proliferazione leucocitaria e che, semmai, il trattamento superficiale riduce debolmente la proliferazione a riposo del PMBCs (*p<0.01; Mann-Whitney U Test).
Una delle qualità richieste ad un materiale utilizzato per la produzione di protesi o dispositivi sanitari, quali i cateteri, è che esso non possegga proprietà attivanti (direttamente o indirettamente) la proliferazione leucocitaria. A tale riguardo, i trattamenti superficiali qui analizzati, sono conformi a tale specifica non presentando capacità attivanti la proliferazione leucocitaria. Semmai, la blanda azione inibitoria potrebbe risultare utile nel limitare un'attivazione indesiderata.
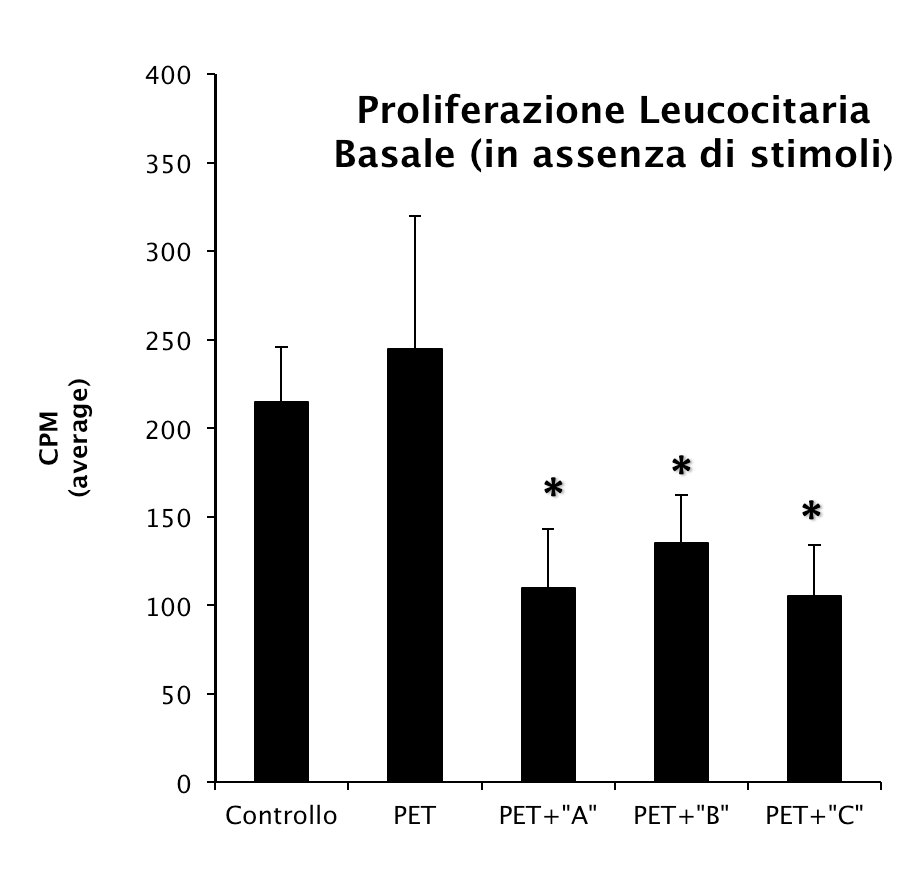
La figura 2 mostra i livelli di incorporazione di timidina tritiata in cellule PBMC stimolate con lipopolisaccaride (costituente le pareti esterne dei batteri Gram-Negativi; LPS) e coltivate per 60 ore in presenza di un prisma di Polietilene Tereftalato (PET) adagiato sul fondo del pozzetto. Il controllo ed i trattamenti dei prismi di PET sono identici a quanto illustrato in figura 1.
Il livello di incorporazione di timidina tritiata indica che i PBMCs, stimolati con LPS, vanno incontro ad una notevole proliferazione (confronta i CPM basali: 215 con i CPM dopo stimolo: 135.000). La presenza del prisma di PET non modifica la risposta proliferativa indotta da LPS (confronta Controllo e PET). La stimolazione dei PBMCs con LPS in presenza dei prismi recanti il trattamento superficiale induce una proliferazione cellulare, misurata come quantità di timidina incorporata, significativamente inferiore (*p<0.01; Mann-Whitney U Test). I dati evidenziano come i trattamenti superficiali qui analizzati non potenzino l'attivazione dei PBMCs prodotta da LPS e mostrino una blanda ma significativa azione inibitoria che potrebbe rivelarsi utile nel limitare l'attivazione leucocitaria indesiderata.
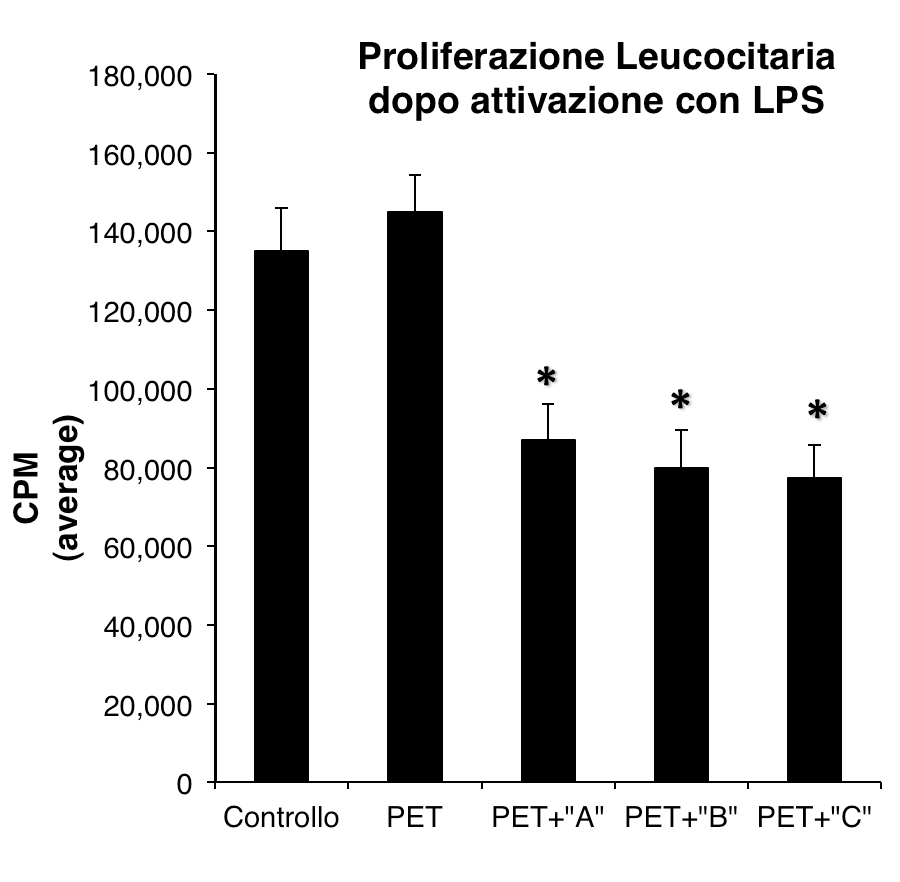
La figura 3 mostra i livelli di incorporazione di timidina tritiata in cellule PBMC stimolate con un anticorpo monoclonale in grado di attivare i linfociti T (OkT3) e coltivate per 60 ore in presenza di un prisma di Polietilene Tereftalato (PET) adagiato sul fondo del pozzetto. Il controllo ed i trattamenti dei prismi di PET sono identici a quanto illustrato in figure 1 e 2.
In sintesi, i dati mostrati indicano che le sostanze in esame non sono in grado di attivare i leucociti né di sinergizzare con stimoli noti e che, al contrario, inducono una lieve soppressione della proliferazione sia in condizioni basali che indotte.
Test di attivazione linfocitaria: questo test ha misurato l'attivazione dei linfociti T CD4+ presenti in campione di PBMC ottenuti da donatori sani. L'espressione dei marcatori di differenziazione è stata misurata mediante citofluorimetria e la percentuale di CD4+ ed il livello di espressione di ogni singolo marcaore è stata valutata mediante analisi bivariata. Gli esperimenti sono stati codotti su PBMCs esposti ai soli prismi di PET (con e senza trattamento superficiale) oppure su cellule attivate con OkT3.
I dati indicano che i PET trattati con stratificazione di tipologia "B" riducono lievemente la quota di linfociti helper attivati. Nessuna delle superfici trattate possiede evidenti attività attivante i linfociti helper presenti nei campioni di PBMCs.
In tutte le condizioni studiate si osserva una buona attivazione linfocitaria misurata come espressione del marcatore CD69.
In tutte le condizioni studiate si osserva una buona attivazione linfocitaria misurata come espressione del marcatore CD71.
In tutte le condizioni studiate si osserva una buona attivazione linfocitaria misurata come espressione del marcatore CD25.
Nessuna delle superfici trattate si è dimostrata in grado di inibire significativamente l'attivazione indotta dal trattamento con OkT3. Solo per i campioni esposti, durante l'attivazione, a superfici con trattamento di tipologia "B" si osserva una modesta riduzione della quota percentuale di linfociti CD4+CD25+. Questa diminuzione non è di entità tale da essere considerata clinicamente rilevante in quanto rientra nella variabilità sperimentale.
I risultati indicano che l'esposizione a superfici di PET trattate con statificazioni nanometriche di Ag/PEO-Like, in assenza di stimoli, aumenta lievemente la popolazione di linfociti Treg (regolatori) CD25+ e che la sostanza B dimostra una attività significativa nel ridurre la popolazione basale di cellule CD69+. Infine le tre sostanze dimostrano una blanda azione inibente l'attivazione linfocitaria indotta dallo stimolo OkT3.
Attività sperimentali su specifici prodotti industriali
CATETERI URINARI: è stato allestito un primo lotto prototipale di cateteri urinari standard ricoperti con il coating in corso di brevettazione internazionale, con proprietà antibatteriche, non-fouling e di elevata lubricità. Tali prototipi sono attualmente in fase di validazione clinica presso una importante Azienda Ospedaliera pubblica.
LENTINE A CONTATTO: è stato allestito un primo lotto prototipale di lentine a contatto, comprendente campioni di lenti semirigide, lenti morbide 38% Polymacon, lenti Ortok e lenti speciali per cheratocono. Su tali campioni è stato applicato il coating in corso di brevettazione internazionale, con proprietà antibatteriche, non-fouling e di elevata lubricità; in questo caso verrà testata anche un implemento della permeabilità all’ossigeno. I prototipi sono attualmente in fase di validazione applicativa da parte di un primario Centro ottico, produttore di lenti speciali e sperimentali, affiancato dalla Clinica Oculistica dell’Università del Molise. E’ in corso di allestimento un secondo lotto prototipale per l’approfondimento della sperimentazione in corso.
FILTRI PER CONDIZIONATORI D’ARIA: è in fase di organizzazione una sperimentazione su filtri di condizionatori di aria impiegati in ambienti molto affollati, quali le aule universitarie.
FILTRI PER CONDIZIONATORI D’ARIA: per camere bianche o camere operatorie: è in fase di organizzazione una sperimentazione analoga alla precedente su filtri a cui viene richiesta una garanzia antibatterica di particolare severità.
ALTRI PRODOTTI INDUSTRIALI: a richiesta di Aziende interessate possono venire attivate linee di ricerca e di trasferimento tecnologico per una gamma molto estesa di prodotti, come illustrato nella parte introduttiva relativa alle competenze di MEDIPLASMA Srl.

